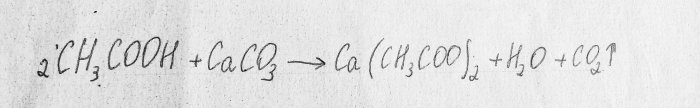О нём-то и пойдёт речь в данной статье. Замечу, что со спиртом это вещество объединяет только название - в этом мы убедимся позже. А сейчас давайте его приготовим!
Понадобится
В качестве химических реактивов будем использовать то, что можно без труда отыскать на прилавках.
Итак, для приготовления твёрдого спирта нам понадобится:
- Уксусная кислота 70%, продаётся в продуктовых магазинах;
- Мел природный - в магазинах для дачи;
- Спирт медицинский 95% либо изопропиловый спирт - в аптеке либо в автомагазине соответственно.
Также нам понадобится немного воды и одноразовая (либо химическая) посуда для проведения самого эксперимента, и резиновые перчатки. Ни в коем случае после завершения опытов Не используйте ничего из вышеперечисленного в пищу!
В качестве мерного стакана можно использовать пластиковый стаканчик на 200 мл.
Приступим к изготовлению сухого спирта
Вначале в колбу прильём 60мл уксусной кислоты и 125 мл воды.
Теперь в полученный раствор небольшими порциями добавляем мел. Начинают выделяться пузырьки газа, при этом важно постоянно помешивать раствор, чтобы они успевали лопаться.
Общий расход мела составит 42 грамма, однако его следует добавлять, пока он не перестанет растворяться.
Рассмотрим химическую реакцию процесса:
Это реакция нейтрализации.
Первое вещество - это уксусная кислота. Второе - карбонат кальция, который содержится в меле. Результатом данной реакции является углекислый газ, вода и ацетат кальция. Данное вещество плохо растворимо в воде, поэтому в ходе эксперимента раствор может затвердеть на глазах:В таком случае необходимо добавить чуть воды и продолжить эксперимент.
Когда кислоты в растворе не останется, реакция прекратится. Даём ему отстояться.
Через некоторое время лишний мел осядет на дно, так как сам по себе он нерастворим в воде. Теперь фильтруем раствор:Я воспользовался бумажным фильтром, также можно использовать ватный диск.
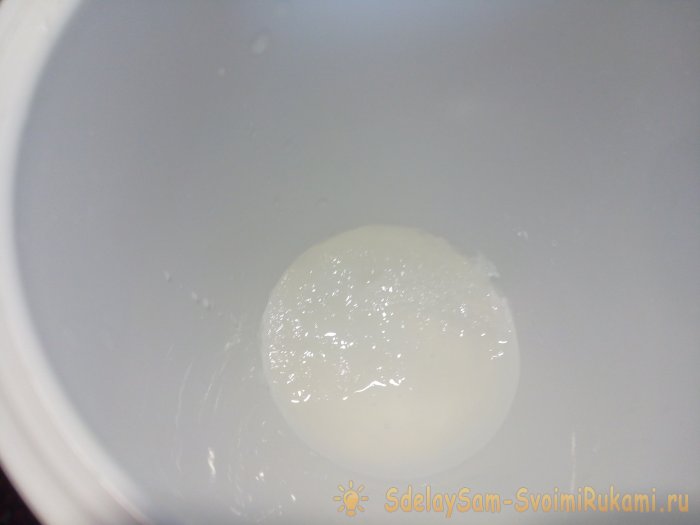
Отфильтрованный раствор имеет желтоватый оттенок, это более-менее чистый раствор ацетата кальция. Переливаем небольшое количество в другую ёмкость и приливаем немного спирта. Начинает образовываться желеобразная масса:
Либо более светлого оттенка:
Поздравляю, мы получили твёрдый спирт! На самом же деле ацетат кальция из-за присутствия спирта, который мы прилили, начал выпадать в осадок в виде моногидрата; ибо спирт имеет свойство вытеснять соли двухвалентных металлов из раствора, что мы и наблюдаем.
Теперь руками (обязательно в перчатках!) придаём нашему желе форму куба либо шара.
При температуре 160 градусов по Цельсию ацетат кальция разлагается, в частности - на легкогорючие вещества, которые способствуют дальнейшему разложению и поддерживают пламя.
Кусочек такого размера способен гореть до шести минут, что является довольно хорошим результатом. А двух кусочков хватит для заварки чая на одного человека. В результате опыта получилось достаточное количество ацетата кальция, а это значит, что его хватит надолго.
Заключение
После изготовления помещаем твёрдый спирт необходимой формы в герметично закрывающуюся тару и смело берём с собой в поход. А на этом данная статья подошла к концу. Всем приятных походов!
P.S. Также из ацетата кальция можно выращивать бесцветные кристаллы иглообразной формы, однако это совсем другая история...